3C-E
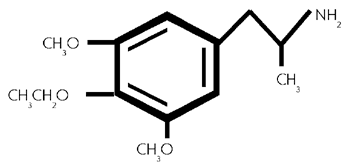
Formel aus:
(42/519)
Andere Namen:
3,5-Dimethoxy -4- ethoxyamphetamin. (42/519)
Allgemeines:
Das Halluzinogen 3C-E ist von der chemischen Struktur betrachtet ein Amphetamin. Shulgin beruecksichtigt dies auch bei der Bennenung. Er verwendet die Vorsilbe 3C- um darauf hinzuweisen, dass es ein Amphetamin ist, welches eben 3 Kohlenstoffatome in der Seitenkette hat. Das E in Namen der Verbindung steht fuer die Ethoxygruppe, den Substituenten an der 4. Position. Halluzinogene Amphetamine gibt es viele und 3C-E ist damit chemisch nahe mit einer Reihe anderer Halluzinogene, wie DOB, DOC oder auch DOM verwandt. Die einzelnen halluzinogenen Amphetamine unterscheiden sich voneinander nur die verschiedene Beschaffenheit der Substituenten am aromatischen Benzolring. Die hier behandelte Rauschdroge 3C-E hat beispielsweise eine Ethoxygruppe an der 4. Position und jeweils eine Methoxygruppe an der 3. und 5. Position. DOB hat hingegen ein Bromatom an der 4. Position, jedoch auch jeweils eine Methoxygruppe an der 3. und 5. Positon. (eigen)
Halluzinogene Amphetamine sind fast immer staerker wirksam als ihre Phenethylamingegenstuecke. Der einzige Unterschied zwischen einem Phenethylamin und einem Amphetamin ist, dass bei den Amphetaminen eine zusaetzliche Methylgruppe in der Seitenkette angebracht ist. Aus der Ethylamingruppe wird ein Isopropylamin. (eigen)
A. Shulgin gibt noch ein kleines Nebenkommentar in seinem Buch "PHIKAL" an, dass 3C-E zwar eine faszinierende Verbindung ist, aber fuer die meisten mit zuvielen Koerperproblemen verbunden ist. (42/520f.)
Wirkungen:
A. Shulgin veroeffentlicht in seinem Buch "PHIKAL" folgende subjektiven Wirkungsbeschreibungen:
40 mg: Es entwickelte sich in etwas Fremdes und Undefinierbares. Es war 'unweltlich'. Ich habe mich unter Kontrolle, aber mit einem Unterton des Unrealen, der mich ein wenig an hohe Dosen LSD erinnert. Wenn es eine grosse Steigerung der sensorischen Aufnahme gab, wollte ich sie nicht sehen. Und wenn ich in kompletter sensorischer Ruhe waere, wuerde ich es vermissen. Aber gerade dort wo ich bin, kann ich sie sehen. Ein unheimlicher Bewusstseinszustand. Und nach der achten Stunde bin ich nuechtern, mit keinem Rest, ausgenommen etwas leichtem Zaehnemahlen.
60 mg: Das Visuelle ist sehr stark, hartnaeckig. Koerperunannehmlichkeiten bestehen sehr stark in der ersten Stunde. Das Gefuehl einer giftigen Buerde besteht eine zeitlang. Ich fuehlte auf Gedeih und Verderben unbequeme koerperliche Wirkungen, Schwaeche oder vor-Uebelkeit, ein starkes Gefuehl des Zitterns (obwohl das Zittern aktuelle relativ leicht war) und allgemeines Unwohlsein, nicht einfach. Ich legte mich hin, um es bequem wie nur moeglich zu haben. Die Phantasie wurde ausgesprochen stark. Zuerst, keine Bilder mit geschlossenen Augen, und sicherlich anti-erotisch. In der 2.ten Stunde der Erfahrung gab es helle Farben, ausgepraegte Schatten, juwelen-artig, mit geschlossenen Augen. Ploetzlich wurde es klar erotisch. Das war das Ende meines schlechten Zustands, und ich schoss ploetzlich auf ein 3+. Komplizierte Phantasien entwickelten sich. Es ist schwer zu wissen, was real und was Phantasie ist. Fortgesetzt erotisch. Am naechsten Morgen sah ich schwach flimmernde Lichter beim Hinausschauen aus den Fenstern. (42/520)
Dosis:
A. Shulgin gibt in seinem Buch "PHIKAL" den Dosisbereich mit 30-60 mg an.(42/520)
Wirkdauer:
Die Dauer der halluzinogenen Wirkung betraegt nach A. Shulgin�s Werk "PHIKAL" 8-12h. (42/520)
Sucht:
Die Ausbildung einer koerperlichen Abhaengigkeit ist nicht bekannt. (eigen)
Synthese:
A. Shulgin gibt in seinem Werk "PHIKAL" folgendes Herstellungsverfahren an:
Eine Loesung von 3,6g Syringaldehyd (3,5-Dimethoxy -4- hydroxybenzaldehyd) in 50 ml MeOH wird mit einer Loesung von 3,7g 85%-igem KOH in 75ml warmem MeOH zusammengefuegt. Diese klare Loesung bildet ploetzlich das Kaliumsalz, zu viel davon um befriedigend zu ruehren. Zu dieser Loesung werden 7,4g Ethyljodid gegeben. Die Mischung wurde auf Rueckflusskochtemperatur mit einem Heizmantel gehalten. Die Feststoffe lockerten und loesten sich, worauf sich eine klar bernsteinfarbene, leichtkochende Loesung ergab. Es wurde weitere 2 Tage am Rueckfluss gekocht. Dann wurden alle fluechtigen Stoffe unter Vakuum entfernt. Der Rest wurde in 400 ml H20 geloest, mit 25%-iger NaOH stark basisch gemacht und mit 4x100 ml CH2Cl2 extrahiert. Die gesammelten Extrakte wurden mit gesaettigter Salzsohle gewaschen. Die Loesungsmittel wurden unter Vakuum entfernt, um 3,3g blassbernsteinfarbenes Oel zu ergeben, welches Kristalle aus 3,5-Dimethoxy-4-ethoxy-benzaldehyd, mit einem mp von 47-48 Grad Celsius, bildete. Ein kleiner Teil wurde aus MeOH umkristallisiert. Dieser hatte einen mp von 48-49 Grad Celsius.
Eine Loesung von 3,3g 3,5-Dimethoxy -4- ethoxy- benzaldehyd in 25ml Nitroethan wurde mit 0,5g wasserfreiem Ammoniumacetat versetzt und 36h am Dampfbad erhitzt. Die Loesungsmittel/Reagentien wurden unter Vakuum entfernt, was ein dickes, gelboranges Oel ergab, welches in 2 Volumen heissen MeOH geloest wurde. Als dieses abkuehlte, erschienen ploetzlich Kristalle. Nach kurzem Kuehlem im Eisbad, wurden diese durch Filtration entfernt, und nochmal mit kaltem MeOH gewaschen, luftgetrocknet bis zum konstanten Gewicht von 2,2g 1- (3,5-Dimethoxy -4- ethoxyphenyl) -2- nitropropen, mit einem mp von 84-85 Grad Celsius. Die Mutterloesungen ergaben beim Stehen ueber Nacht grosse Klumpen von kristallinen Material, welche dekantiert wurden. Sie wurden dann unter einer kleinen Menge MeOH gemahlen, dann aus 60%-igen EtOH rekristallisiert. Eine 2. Menge von 0,7g des Nitrostyrens wurde so erhalten, als kanariengelbe Kristalle mit einem mp von 83-85 Grad Celsius.
Eine Loesung von 2,7g 1- (3,5-Dimethoxy -4- ethoxyphenyl) -2- nitropropen in 20 ml wasserfreiem THF wurde zu einer Suspension von 2g LAH in 150 ml warmen THF hinzugefuegt. Die Mischung wurde am Rueckfluss 48h lang am Kochen gehalten. Nach 48-stuendigem Ruehren bei Raumtemperatur wurde das ueberschuessige Hydrid zerstoert, durch Zugabe von 2ml H20 in 10 ml THF, gefolgt von 2ml 15%-iger NaOH und nochmal 6ml H2O. Die anorganischen Salze wurden durch Filtration beseitigt. Der Filterkuchen wurde mit THF gewaschen. Die vereinigten Mutterlaugen und Waschungen wurdem vom Loesungsmittel unter Vakuum befreit, bis ein gelbes Oel zurueckblieb mit etwas ungeloestem anorganischen Salz in sich. Dies wurde in 300 ml CH2Cl2 geloest, mit verd. NaOH gewaschen, und mit 3x150 ml 1N HCl extrahiert. Die gesammelten Extrakte wurden 1x mit CH2Cl2 gewaschen, mit 25%-iger NaOH basisch gemacht, und mit 3x100 ml CH2Cl2 extrahiert. Die kombinierten Organika wurden mit gesaettigter NaCl-Loesung gewaschen. Die Loesungsmittel wurden unter Vakuum entfernt, um rund 2ml farbloses Oel zu erhalten. Dies wurde in 10 ml IPA geloest, mit konz. HCl (10 Tropfen wurden gebraucht) neutralisiert und mit 125ml wasserfreiem Et2O verduennt. Die leichte Woelkigkeit entwickelte sich zur Bildung von feinen, weissen Kristallen. Nach Stehen bei Raumtemperatur, 2h lang, wurden diese entfernt, mit Diethylether gewaschen, und luftgetrocknet. Es wurden 1,9g 3C-E-HCl, als brilliant weisse Kristalle, erhalten. (42/519f.)